выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
Внешний вид:
серебристо-бел. кубические металл
Кристаллические модификации, цвет растворов и паров:
Температуры перехода из альфа (кубическая) в бета (гексагональная) 215 С, из бета в гамма (кубическая) 605 С.
Брутто-формула (система Хилла): Sr
Формула в виде текста: Sr
Молекулярная масса (в а.е.м.): 87,62
Температура плавления (в °C): 768
Температура кипения (в °C): 1390
Растворимость (в г/100 г или характеристика):
аммиак жидкий: растворим
вода: реагирует
Плотность:
2,63 (20°C, г/см3)
Давление паров (в мм.рт.ст.):
0,01 (533°C)
0,1 (621°C)
1 (733°C)
10 (877°C)
100 (1097°C)
Удельная теплоемкость при постоянном давлении (в Дж/г·K):
0,31 (25°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
0 (т)
Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль):
0 (т)
Стандартная энтропия образования S (298 К, Дж/моль·K):
53,1 (т)
Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):
27,2 (т)
Энтальпия плавления ΔHпл (кДж/моль):
9,2
Энтальпия кипения ΔHкип (кДж/моль):
141,4
Аналитические
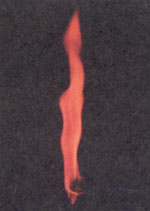 Соли стронция окрашивают пламя в карминово-красный цвет (на фото). Соли стронция окрашивают пламя в карминово-красный цвет (на фото).
Дополнительная информация:
Медленно реагирует с концентрированной серной кислотой. На воздухе быстро покрывается пленкой оксидов и нитридов. При нагревании легко реагирует с водородом образуя гидрид стронция. Быстро реагирует с водой с выделением водорода и образованием гидроксида стронция. Легко растворяется в минеральных кислотах с выделением водорода, при реакции с разбавленной азотной кислотой в значительных количествах образуется нитрат аммония и водород. При нагревании с галогенами дает галогениды. Содержание элемента в земной коре 0,04%.
Источники информации:
- "Энциклопедия для детей" т.17: Химия, М.:Аванта+, 2004 стр. 195
- Гурвич Я.А. "Справочник молодого аппаратчика-химика" М.:Химия, 1991 стр. 51
- Карапетьянц М.Х., Дракин С.И. "Общая и неорганическая химия" М.:Химия 1981 стр. 309-316
- Рабинович В.А., Хавин З.Я. "Краткий химический справочник" Л.: Химия, 1977 стр. 99
См. также статью "Ўтронций" в Химической энциклопедии.
выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
|
 Соли стронция окрашивают пламя в карминово-красный цвет (на фото).
Соли стронция окрашивают пламя в карминово-красный цвет (на фото).