Без присутствия водорода натрий не реагирует с кислородом.Sovetnik писал(а):натрий легче провзаимодействует с кислородом, чем с водородом.
Его можно даже перегнать в атмосфере сухого кислорода.
Без присутствия водорода натрий не реагирует с кислородом.Sovetnik писал(а):натрий легче провзаимодействует с кислородом, чем с водородом.
Это при атмосферном давлении водородаstallker писал(а):Гидрид натрия при атмосферном давлении без плавления разлагается при температуре выше 420 С.
Как будет вести себя натрий в зависимости от температуры и количества водорода,Droog_Andrey писал(а): Другое дело, что при 420 это будет происходить быстрее.
Натрий, водород и гидрид натрия, в замкнутом сосуде находятся в динамическом равновесии в соответствии с зависимостью давления диссоциации от температуры.stallker писал(а): Как будет вести себя натрий в зависимости от температуры и количества водорода, останется в колбе или улетит в токе водорода?
Гидрид интересен как восстановитель работающий в атмосфере .Sovetnik писал(а):Натрий, водород и гидрид натрия, в замкнутом сосуде
По колен валам обратитесь на металлобрабоку к Николай Павловичу.aleks32jojo писал(а): Нужен совет практика-профи.
скорее как то так?Droog_Andrey писал(а):(навеяно соседней темой)
По идее, сначала алюминий должен съесть остатки влаги:
Al + NaOH + H2O = NaAlO2 + 1,5H2
А затем начать восстанавивать натрий:
Al + 2NaOH = NaAlO2 + Na + H2
Гидрид натрия валится выше 300 градусов, так что его образование маловероятно. Растворимость алюминия в жидком натрии также невелика, так что выход натрия может быть неплохим.
Крайне необходимо предотвратить доступ воздуха, иначе натрий и водород подорвутся, и всё вокруг будет заляпано расплавленной щёлочью, что не очень приятно. Важно также не допускать плавления алюминия, чтобы натрий не загрязнялся им и не улетал.
Вопрос в том, насколько быстро пойдёт восстановление при умеренных температурах (450-500 градусов)? Пробовать как-то стрёмно...
И тут пытаетесь с умным видом поддеть.Alex K писал(а):скорее как то так?
2Al + 6NaOH = NaAlO2 + Na5AlO4 + 3H2
http://pubs.rsc.org/en/content/articlep ... 9840001139Droog_Andrey писал(а):И тут пытаетесь с умным видом поддеть.Alex K писал(а):скорее как то так?
2Al + 6NaOH = NaAlO2 + Na5AlO4 + 3H2
Вообще-то, эту реакцию (Al + NaOH распл.) обычно на "ортоалюминат" (Na3AlO3) пишут. А в той же статье есть, например, Na17Al5O16, что вполне к ортоалюминату близко...Droog_Andrey писал(а):В статье стандартное для таких случаев (богатые ЩМ фазы типа K6CdO4, ортонитратов и т.п.) многосуточное спекание без следов водорода (он разрушает многозарядные кислородные анионы с отщеплением от них воды или OH¯).
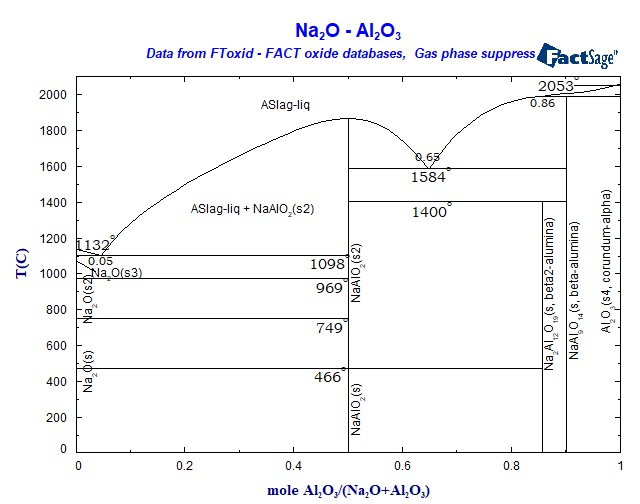
У нас же намного менее экзотические условия, а водорода более чем дохрена. Так что смотрим на обычную диаграмму Na2O+Al2O3 и понимаем, что ничего, кроме NaAlO2, нам тут не светит.
Ни разу не видел.Alex K писал(а):обычно на "ортоалюминат" (Na3AlO3) пишут
Да пишут-пишут. Правда, только в школьных учебниках, чтобы с уравниванием не заморачиваться: 6 NaOH + 2 Al ---> 2 Na3AlO3 + 3 H2Droog_Andrey писал(а):Ни разу не видел.Alex K писал(а):обычно на "ортоалюминат" (Na3AlO3) пишут
Сейчас этот форум просматривают: Baidu [Spider] и 5 гостей